Руководство для врача Скорой Помощи
ГЛАВА 5
СИНДРОМЫ И НЕОТЛОЖНЫЕ ЗАБОЛЕВАНИЯ ОРГАНОВ ДЫХАНИЯ.
5.1 ОБОСТРЕНИЕ БРОНХИАЛЬНОЙ АСТМЫ
ОПРЕДЕЛЕНИЕ
Бронхиальная астма - это заболевание, в основе которого лежит хроническое аллергическое воспаление и гиперреактивность бронхов, клинически проявляющееся бронхиальной обструкцией, изменяющейся с течением времени. Повторные эпизоды, навязчивый непродуктивный кашель, особенно ночью и/или ранним утром - это симптомы распространенной, но вариабельной обструкции бронхиального дерева, частично обратимой спонтанно или исчезающей под влиянием лечения.
Известны 4 механизма обструкции дыхательных путей:
- спазм гладких мышц;
- отек слизистой дыхательных путей;
- гиперсекреция с образованием слизистых пробок;
- склероз стенки бронхов при длительном и тяжелом течении заболевания.
Таким образом БА представляет собой хроническое, аллергическое воспаление дыхательных путей, приводящее к гиперреактивности бронхов, их обструкции вследствие бронхоконстрикции, отека слизистой и обтурации вязким секретом, клинически проявляющееся респираторными симптомами.
Диагностические критерии БА
Диагноз БА на догоспитальном этапе ставится на основании жалоб, анамнеза заболевания и клинического обследования.
1. Жалобы и анамнез заболевания.
Наличие приступов удушья или одышки, появление свистящих хрипов, кашля и их исчезновение спонтанно или после применения бронходилататоров и противовоспалительных препаратов. Связь этих симптомов с факторами риска БА (см. факторы риска БА). Наличие в анамнезе у больного или его родственников установленной БА или других аллергических заболеваний.
2. Клиническое обследование.
Вынужденное положение, участие вспомогательной дыхательной мускулатуры в акт дыхания, сухие хрипы, которые слышны на расстоянии и/или при аускультации над легкими.
При наличии (в том числе и у больного) пикфлоуметра или спирометра регистрируется значительная бронхообструкция - объем форсированного выдоха за 1сек (ОФВ1) или пиковая скорость выдоха (ПСВ) менее 80% от должных или нормальных значений.
Критерии обострения БА
Обострение БА может протекать в виде острого приступа или затяжного состояния бронхиальной обструкции.
Приступ БА - остро развившееся и/или прогрессивно ухудшающееся экспираторное удушье, затрудненное и/или свистящее дыхание, спастический кашель, или сочетание этих симптомов, при резком снижении показателя пиковой скорости выдоха.
Обострение в виде затяжного состояния бронхиальной обструкции характеризуется длительным (дни, недели, месяцы) затруднением дыхания, с клинически выраженным синдромом бронхиальной обструкции, на фоне которого могут повторяться острые приступы БА различной тяжести.
Обострения бронхиальной астмы являются ведущей причиной вызовов “скорой помощи” и госпитализации пациентов.
Оценка обострения БА проводится по клиническим признакам и (при наличии пикфлоуметра) функциональным дыхательным пробам. Обострение по степени тяжести может быть легким, среднетяжелым, тяжелым и в виде астматического статуса.
Таблица 1. Классификация тяжести обострения БА*.
|
Степень тяжести |
Легкая |
Средней тяжести |
Тяжелая |
Астматическое состояние |
|
Симптомы |
||||
|
Физическая активность |
Сохранена |
Ограничена |
Резко снижена, вынужденное положение |
Резко снижена или отсутствует |
|
Сознание |
Не изменено, иногда возбуждение |
Возбуждение |
Возбуждение, испуг, «дыхательная паника» |
Спутанность сознания, коматозное состояние |
|
Речь |
Сохранена |
Ограничена, произносит отдельные фразы |
Речь затруднена |
Отсутствует |
|
Нормальные показатели частоты дыхания у бодрствующих детей (ЧД в мин) |
||||
|
Частота дыхания |
Нормальная или учащенное до 30% нормы |
Выраженная экспираторная одышка . Более 30-50% от нормы |
Резко выраженная экспираторная одышка более 50% от нормы |
Тахипноэ или брадипноэ |
|
Участие вспомогательных дыхательных мышц;
|
Не резко выражено |
Выражено |
Резко выражено |
Парадоксальные торако-абдоминальные дыхание |
|
Дыхание при аускультации |
Свистящие хрипы, обычно в конце выдоха |
Выраженное свистящее на вдохе и на выдохе или мозаичное проведение дыхания |
Резко выраженное свистящее или ослабление проведения |
Отсутствие дыхательных шумов,“немое легкое” |
|
Нормальные показатели частоты пульса у бодрствующих детей (уд/мин) |
||||
|
Частота пульса |
увеличена |
увеличена |
Резко увеличена |
Брадикардия |
|
ПСВ** (% от нормы или лучшего индивидуального показателя) |
70-90% |
50-70% |
<50% |
<30% |
|
Частота приема бронхолитиков в последние
|
Не использовались или использовались низкие/средние дозы. Эффективность недостаточная, возросла потребность по сравнению с индивидуальной нормой |
Использовались высокие дозы. |
||
|
РаСО2 *** мм/рт.ст. |
35 |
35-45 |
40 |
|
|
SaO2*** |
95 |
90-95 |
90 |
* - На тяжесть обострения указывает наличие хотя бы нескольких параметров
** - ПСВ - используется у взрослых и детей старше 5 лет
***-В настоящее время определяется преимущественно в стационаре
Таблица 2. Нормативы показателей функции внешнего дыхания у детей
| Рост, см | ОФВ1 (л) | ПСВ (л/мин) | Рост, см | ОФВ1 (л) | ПСВ (л/мин) |
| 100 | 0,84 | 98 | 122 | 1,46 | 214 |
| 101 | 0,86 | 103 | 123 | 1,46 | 219 |
| 102 | 0,88 | 109 | 124 | 1,53 | 224 |
| 103 | 0,91 | 114 | 125 | 1,56 | 229 |
| 104 | 0,93 | 119 | 126 | 1,60 | 235 |
| 105 | 0,96 | 124 | 127 | 1,63 | 240 |
| 106 | 0,98 | 130 | 128 | 1,67 | 245 |
| 107 | 1,01 | 135 | 129 | 1,71 | 250 |
| 108 | 1,04 | 140 | 130 | 1,74 | 255 |
| 109 | 1,06 | 145 | 131 | 1,78 | 261 |
| 110 | 1,09 | 151 | 132 | 1,82 | 266 |
| 111 | 1,12 | 156 | 133 | 1,86 | 271 |
| 112 | 1,15 | 161 | 134 | 1,90 | 276 |
| 113 | 1,18 | 166 | 135 | 1,94 | 282 |
| 114 | 1,21 | 172 | 136 | 1,98 | 287 |
| 115 | 1,24 | 177 | 137 | 2,02 | 292 |
| 116 | 1,27 | 182 | 138 | 2,06 | 297 |
| 117 | 1,30 | 187 | 139 | 2,10 | 303 |
| 118 | 1,33 | 193 | 140 | 2,14 | 308 |
| 119 | 1,36 | 198 | 141 | 2,19 | 313 |
| 120 | 1,39 | 203 | 142 | 2,23 | 318 |
| 121 | 1,43 | 208 |
Тактика догоспитальной терапии полностью определяется степенью выраженности обострения БА, поэтому при формулировке диагноза врачом СС и НМП необходимо указывать степень тяжести обострения БА.
Тактика врача при лечении приступа бронхиальной астмы имеет несколько общих принципов:
При осмотре врачу необходимо по клиническим данным оценить степень тяжести обострения, определить ПСВ (при наличии пикфлоуметра).
При возможности ограничить контакт с причинно-значимыми аллергенами или триггерами.
По данным анамнеза уточнить ранее проводимое лечение:
бронхоспазмолитические препараты, пути введения; дозы и кратность назначения;
время последнего приема препаратов; получает ли больной системные кортикостероиды, в каких дозах.
Исключить осложнения (например, пневмонию, ателектаз, пневмоторакс или пневмо-медиастинум).
Оказать неотложную помощь в зависимости от тяжести приступа.
Оценить эффект терапии (одышка, ЧСС, АД. Прирост ПСВ>15%).
Выбор препарата, дозы и пути введения
Современное оказание помощи больным при обострении БА подразумевает применение только следующих групп лекарственных средств:
1. Селективные бета-2-агонисты адренорецепторов короткого действия (сальбутамол, фенотерол).
2. Холинолитические средства (ипратропиум бромид); их комбинированный препарат беродуал (фенотерол + ипратропиум бромид).
3. Глюкокортикоиды.
4. Метилксантины.
Селективные бета-2-агонисты короткого действия.
Эти препараты, обладая бронхоспазмолитическим действием, являются препаратами первого ряда при лечении приступов БА.
САЛЬБУТАМОЛ (вентолин, сальбен, небулы вентолина и 0,1% раствор сальгима для небулайзерной терапии) - селективный агонист бета-2 адренорецепторов.
Бронхорасширяющий эффект сальбутамола наступает через 4-5 минут. Действие препарата постепенно возрастает до своего максимума к 40-60 минуте. Период полувыведения 3-4 часа, а продолжительность действия составляет 4-5 часов.
Способ применения: С помощью небулайзера небулы по 2,5 мл, содержащая 2,5 мг сальбутамола сульфата в физиологическом растворе. Назначаются 1-2 небулы (2,5 - 5,0 мг) на ингаляцию в неразбавленном виде. Если улучшения не наступает, проводят повторные ингаляции сальбутамола по 2,5 мг каждые 20 минут в течение часа. Кроме того препарат используется в виде ДАИ (спейсера), спейсера или дискхайлера (100 мкг на ингаляцию по 1-2 вдоха) или циклохайлера (200 мкг на ингаляцию по 1 вдоху).
ФЕНОТЕРОЛ (беротек) и раствор беротека для небулайзерной терапии - селективный бета-2-агонист короткого действия. Бронхолитический эффект наступает через 3-4 минуты и достигает максимума действия к 45 минуте. Период полувыведения 3-4 часа, а продолжительность действия фенотерола составляет 5-6 часов.
Способ применения: С помощью небулайзера - по 0,5-1,5 мл раствора фенотерола в физиологическом растворе в течение 5-10 минут. Если улучшения не наступает, проводят повторные ингаляции той же дозы препарата каждые 20 минут. Детям 0,5 -1,0 мл (10-20 капель) на 1 ингаляцию. Используется беротек также в виде ДАИ (100 мкг по 1-2 вдоху).
Побочные эффекты. При применении бета-2-агонистов возможны тремор рук, возбуждение, головная боль, компенсаторное увеличение ЧСС, нарушения ритма сердца, артериальная гипертензия. Побочные эффекты более ожидаемы у больных с заболеваниями сердечно-сосудистой системы, в старших возрастных группах и у детей; при неоднократном применении бронхоспазмолитика, зависят от дозы и способа введения препарата.
Относительные противопоказания к применению ингаляционных бета-2-агонистов - тиреотоксикоз, пороки сердца, тахиаритмия и выраженная тахикардия, острая коронарная патология, декомпенсированный сахарный диабет, повышенная чувствительность к бета-адреномиметикам.
Холинолитические средства
ИПРАТРОПИУМ БРОМИД (атровент) - антихолинергическое средство с очень низкой, (не более 10%) биодоступностью, что обуславливает хорошую переносимость препарата. Ипратропиум бромид применяется в случае неэффективности бета-2-агонистов, как дополнительное средство с целью усиления их бронхолитического действия, при индивидуальной непереносимости бета-2-агонистов, с у больных с хроническим бронхитом.
Способ применения: Ингаляционно - с помощью небулайзера - по 1,0 - 2,0 мл (0,25- 0,5 мг). При необходимости повторяют через 30-40 мин.С помощью ДАИ или спейсера 40-80 мкг.
Комбинированные препараты
БЕРОДУАЛ - комбинированный бронхоспазмолитический препарат, содержащий два бронхорасширяющих вещества фенотерол и ипратропиум бромид. Одна доза беродуала содержит 0,05 мг фенотерола и 0,02 мг ипратропиума бромида.
Способ применения: С помощью небулайзера для купирования приступа ингалируют раствор беродуала 1-4 мл в физиологическом растворе 5-10 минут. Если улучшение не наступает, проводят повторную ингаляцию через 20 минут. Доза препарата разводится в физиологическом растворе. С помощью ДАИ - 1-2 вдоха, при необходимости через 5 минут - еще 2 дозы, последующую ингаляцию проводить не ранее, чем через 2 часа.
Системные глюкокортикоиды
Показания к применению при БА:
тяжелое и жизнеугрожающее обострение БА
купирование приступа удушья у пациента с гормонально-зависимой формой БА
анамнестические указания на необходимость применения глюкокортикоидов для купирования обострения БА в прошлом.
Побочные эффекты: артериальная гипертензия, возбуждение, аритмия, язвенные кровотечения
Противопоказания: Язвенная болезнь желудка и 12-перстной кишки, тяжелая форма артериальной гипертензии, почечная недостаточность.
ПРЕДНИЗОЛОН является дегидрированным аналогом гидрокортизона и относится к синтетическим глюкокортикостероидным гормонам. Период полувыведения 2-4 часа, продолжительность действия 18-36 часов. Вводится парентерально взрослым в дозе не менее 60 мг, детям - парентерально или внутрь 1-2 мг/кг.
МЕТИЛПРЕДНИЗОЛОН (солумедрол, метипред) Негалогеновый производный преднизолона, обладающий большей противовоспалительной (5 мг преднизолона эквивалентны 4 мг метилпреднизолона) и существенно меньшей минералокортикоидной активностью.
Препарат характеризуется коротким, как и у преднизолона, периодом полувыведения, более слабой стимуляцией психики и аппетита. Для терапии обострений бронхиальной астмы используется как и преднизолон, но в меньших дозах (из расчета метилпреднизолон-преднизолон как 4 : 5).
Могут быть эффективны ингаляционные глюкокортикоиды (будесонид). Целесообразно использовать ингаляционные глюкокортикоиды через небулайзер.
Ингаляционные глюкокортикоиды
БУДЕСОНИД (пульмикорт) - суспензия для небулайзера в пластиковых контейнерах 0,25-0,5 мг (2 мл).
При биотрансформации будесонид в печени, образует метаболиты с низкой глюкокортикостероидной активностью.
Пульмикорт суспензию для небулайзера можно разбавлять физиологическим раствором, а также смешивать с растворами сальбутамола и ипратропиума бромида. Доза для взрослых - 0,5 мг (2 мл), детям - 0,5 мг (1 мл) дважды через 30 мин.
Метилксантины
ЭУФИЛЛИН представляет собой комбинацию теофиллина (80%), определяющего фармакодинамику препарата, и этилендиамина (20%), обусловливающего его растворимость. Механизмы бронхолитического действия теофиллина хорошо известны.
При оказании неотложной помощи препарат вводится внутривенно, при этом действие начинается сразу и продолжается до 6-7 часов. Для теофиллина характерна узкая терапевтическая широта, т.е. даже при небольшой передозировке препарата возможно развитие побочных эффектов. Период полувыведения у взрослых - 5-10 часов. Около 90% введенного препарата метаболизируется в печени, метаболиты и неизмененный препарат (7-13%) выделяются с мочой через почки. У подростков и курильщиков метаболизм теофиллина ускорен, что может потребовать увеличения дозы препарата и скорости инфузии. Нарушения функции печени, застойная сердечная недостаточность и пожилой возраст, наоборот, замедляют метаболизм препарата, увеличивают опасность развития побочных эффектов и обусловливают необходимость снижения дозы и уменьшения скорости внутривенной инфузии эуфиллина.
Показания к применению при БА:
купирование приступа БА в случае отсутствия ингаляционных средств или как дополнительная терапия при тяжелом или жизнеугрожающем обострении БА.
Побочные явления:
со стороны сердечно-сосудистой системы - снижение артериального давления, сердцебиение, нарушения ритма сердца, кардиалгии
со стороны желудочно-кишечного тракта - тошнота, рвота, диарея;
со стороны ЦНС - головная боль, головокружение, тремор, судороги.
Взаимодействие (см. табл. 3)
препарат несовместим с раствором глюкозы.
Доза у детей: 4,5-5 мг/кг внутривенно (вводится в течение 20-30 мин) в 10-15 мл физиологического раствора.
Небулайзерная терапия в условиях «скорой помощи»
Цель небулайзерной терапии состоит в доставке терапевтической дозы препарата в аэрозольной форме непосредственно в бронхи больного и получении фармакодинамического ответа за короткий период времени (5-10 минут).
Небулайзерная терапия проводится с помощью специального прибора, состоящего из самого небулайзера и компрессора, создающего поток частиц размером 2-5 мкм со скоростью не менее 4 л/мин.
Слово «небулайзер» происходит от латинского слова nebula, что значит туман. Небулайзер - устройство для преобразования жидкости в аэрозоль с особо мелкодисперсными частицами способными проникать преимущественно в периферические бронхи. Осуществляется данный процесс под воздействием сжатого воздуха через компрессор (компрессорный небулайзер) или под влиянием ультразвука (ультразвуковой небулайзер).
Небулайзерная терапия, создавая высокие концентрации лекарственного вещества в легких, не требует координации ингаляции с актом вдоха, что имеет существенное преимущество перед ДАИ.
Эффективность ингаляций зависит от дозы аэрозоля и определяется рядом факторов:
количеством продуцируемого аэрозоля,
характеристикой частиц,
соотношением вдоха и выдоха,
анатомией и геометрией дыхательных путей
Экспериментальные данные свидетельствуют о том, что оптимальными для попадания в дыхательные пути и соответственно рекомендуемыми к являются аэрозоли с диаметром частиц 2-5 мкм. Более мелкие частицы (менее 0,8 мкм) попадают в альвеолы, где быстро всасываются или выдыхаются, не задерживаясь в дыхательных путях, не обеспечивая терапевтического эффекта. Более крупные частицы (более 10 мкм) оседают в ротоглотке. Благодаря небулайзерной терапии достигается более высокий терапевтический индекс лекарственных веществ, определяющий эффективность и безопасность проводимого лечения.
Основные показания к применению небулайзеров на догоспитальном этапе лечения БА:
необходимость применения высоких доз препаратов;
целенаправленная доставка препарата в дыхательные пути;
если имеют место осложнения при применении обычных доз лекарственных средств и высока частота применения ингаляционных кортикостероидов и других противовоспалительных средств;
у детей, особенно первых лет жизни;
тяжесть состояния (отсутствие эффективного вдоха )
предпочтение больного
Преимущества небулайзерной терапии:
отсутствие необходимости в координации дыхания с поступлением аэрозоля;
возможность использования высоких доз препарата и получение фармакодинамического ответа за короткий промежуток времени;
непрерывная подача лекарственного аэрозоля с мелкодисперсными частицами;
быстрое и значительное улучшение состояния вследствие эффективного поступления в бронхи лекарственного вещества;
легкая техника ингаляций.
Препараты для небулайзерной терапии применяют в специальных контейнерах, небулах, а также растворах, выпускаемых в стеклянных флаконах. Это дает возможность легко, правильно и точно дозировать лекарственное средство.
Техника ингаляции с помощью небулайзера.
Для ингаляции через небулайзер необходимо:
открыть небулайзер;
перелить жидкость из небулы или накапать раствор из флакона (разовую дозу препарата);
добавить физиологический раствор до нужного объема 2-3 мл (по инструкции к небулайзеру;
собрать небулайзер;
присоединить мундштук или лицевую маску;
включить компрессор, соединить небулайзер и компрессор;
выполнить ингаляцию до полного расходования раствора;
У детей предпочтение отдается ингаляции через рот с помощью мундштука;
У детей первых лет жизни можно использовать плотно прилегающую маску.
Первичная санитарная обработка небулайзера осуществляется на подстанции. Для этой цели необходимо разобрать небулайзер, промыть насадки теплой водой с детергентом, просушить (пользоваться щеткой нельзя). В дальнейшем небулайзер и насадки стерилизуются в автоклаве при 120°С и 1,1 атмосфере (ОСТ 12-21-2-85).
Техническая инспекция небулайзеров осуществляется 1 раз в год.
Таблица 3.
Лечение обострения БА на догоспитальном этапе
| Диагноз | Медикаментозная терапия | Результат | |
| У взрослых | У детей | ||
|
БА, Легкий приступ |
вентолин 2,5 мг (1 небула) или сальгим 2,5 мг (1/2 флакона) через
небулайзер в течение 5-10 мин; или беродуал 1-2 мл (20-40 капель) через небулайзер в течение 5-10 мин; Оценить терапию через 20 минут. При неудовлетворительном эффекте повторить аналогичную ингаляцию бронхолитика |
вентолин 1,25-2,5 мг (1/2-1 небула) через небулайзер в течение 5-10 мин
или сальгим 1,25-2,5 мг (1/4-1/2 фл.). или беродуал 0,5 мл - 10 кап. (детям до 6 лет) и 1 мл - 20 капель (детям старше 6 лет) через небулайзер в течение 5-10 мин; Оценить терапию через 20 минут При неудовлетворитель ном эффекте повторить аналогичную ингаляцию бронхолитика. |
1. Купирование приступа |
|
БА, Средне-тяжелое обострение |
вентолин 2,5-5,0 мг (1-2 небулы) или сальгим 2,5-5,0 (1/2-1 фл.) мг через
небулайзер в течение 5-10 мин или беродуал 1-3 мл (20-60 капель) через небулайзер в течение 5-10 мин; и преднизолон перорально 20-30 мг, в/в 60-90мг или метилпреднизолон в/в 40-80 мг; или пульмикорт через небулайзер 1000-2000 мгк (1-2 небулы) в течение 5-10 мин Оценить терапию через 20 минут При неудовлетворительном эффекте повторить аналогичную ингаляцию бронхолитика |
вентолин 2,5 мг (1 небула) через небулайзер в течение 5-10 мин или сальгим
(1/2 фл.) или беродуал 0,5 мл - 10 кап. у детей до 6 лет и 1 мл - 20 капель (у детей старше 6 лет) через небулайзер в течение 5-10 мин; и преднизолон - перорально 20-30 мг; в/в 1 мг/кг или пульмикорт (1/2-1 небула 250-500 мкг) через небулайзер в течение 5-10 мин; Оценить терапию через 20 минут При неудовлетворительном эффекте повторить аналогичную ингаляцию бронхолитика |
1. Купирование приступа 2. Госпитализация детям в стационар |
|
БА, Тяжелое обострение |
вентолин, сальгим или беродуал в тех же дозах и преднизолон перорально 30-60 мг, в/в 90-150 мг (или метилпреднизолон в/в 80-120 мг и пульмикорт через небулайзер 1000-2000 мкг 1-2 небулы в течение 5-10 мин. |
Вентолин или сальгим или беродуал в тех же дозах и преднизолон для детей
- в/в 60-120 мг или перорально 1-2 мг/кг или/и пульмикорт через небулайзер 250-500-1000 мкг в течение 5-10 мин. |
1. Госпитализация в стационар |
|
БА Астматический статус |
вентолин, сальгим или беродуал в тех же дозах и преднизолон в/в 90-150 мг
(или метилпреднизолон в/в 80-120 мг и пульмикорт через небулайзер
1000-2000 мкг 1-2 небулы в течение 5-10 мин.; При неэффективности интубация трахеи, ИВЛ |
вентолин или сальгим или беродуал в тех же дозах и преднизолон для детей
- не менее 60-120 мг в/в или 1-2 мг/кг перорально или пульмикорт через небулайзер в течение 5-10 мин; Интубация трахеи, ИВЛ |
2. Госпитализация в БИТ |
* При неэффективности терапии тяжелой степени обострения и угрозе остановки дыхания возможно введение адреналина взрослым 0,1% - 0,5 мл подкожно. Детям 0,01 мл/ кг но не более 0,3 мл
** При отсутствии небулайзеров или при настойчивой просьбе больного возможно введение эуфиллина 2,4% раствора 10,0-20,0 мл внутривенно в течение 10 минут.
***Признаки, угрожающие жизни: цианоз, немое легкое, ослабление дыхания, общая слабость, у старших детей ПСВ менее 33%. В этом случае немедленная госпитализация, использование бета-2-агонистов в необходимой дозе и частоте, преднизолон внутрь, оксигенотерапия
Критерии эффективности проводимого лечения:
1. «Хорошим» считается ответ на проводимую терапию если:
состояние стабильное, уменьшилась одышка и количество сухих хрипов в легких; ПСВ
увеличилось на 60 л/мин, у детей - на 12-15% от исходного.
2. «Неполным» считается ответ на проводимую терапию если:
состояние нестабильное, симптомы в прежней степени, сохраняются участки с
плохой проводимостью дыхания, нет прироста ПСВ.
3. «Плохим» считается ответ на проводимую терапию если:
симптомы прежней степени или нарастают, ПСВ ухудшается.
Таблица 4. Для лечения бронхиальной астмы
НЕ РЕКОМЕНДУЕТСЯ ПРИМЕНЯТЬ:
|
Психотропные препараты |
угнетение дыхания за счет центрального миорелаксирующего действия |
|
Наркотические анальгетики |
угнетение дыхательного центра |
|
Антигистаминные препараты 1 поколения |
усугубляют бронхообструкцию за счет повышения вязкости мокроты, сродство димедрола к Н1-гистаминовым рецепторам значительно ниже, чем у собственно гистамина, не вытесняется гистамин, уже связавшийся с рецепторами, а имеется лишь профилактическое действие, гистамин не играет ведущей роли в патогенезе приступа бронхиальной астмы. |
|
Массивная гидратация |
Эффект не доказан, показана лишь адекватная регидратация с целью восполнения потерь жидкости с потом или вследствие усиленного диуреза после использования эуфиллина |
|
Нестероидные противоспалительные препараты (аспирин) |
противопоказаны при “аспириновой” астме, риск непереносимости аспирина |
ЧАСТО ВСТРЕЧАЮЩИЕСЯ ОШИБКИ ТЕРАПИИ.
При обострении БА нежелательно использование неселективных бета-агонистов типа ипрадола и астмопента в связи с высоким риском развития побочных эффектов. Для лечения бронхиальной обструкции неэффективны традиционно используемые антигистаминные препараты (димедрол и др.), поскольку их сродство к Н1-гистаминовым рецепторам значительно ниже, чем у собственно гистамина и они не вытесняют гистамин, уже связавшийся с рецепторами. Кроме того, гистамин не играет ведущей роли в патогенезе приступа БА. Использование адреналина, хотя и эффективно, но чревато серьезными побочными эффектами. В настоящее время, когда имеется широкий выбор селективных адреномиметиков, применение адреналина оправданно только для лечения анафилаксии. Применение коргликона необоснованно из-за неэффективности при правожелудочковой недостаточности. Сочетание коргликона с эуфиллином повышает опасность развития дигиталисных аритмий (в том числе желудочковых). Кроме того, нет никакой связи между дозой и влиянием сердечных гликозидов на активность синусового узла, поэтому их действие на ЧСС при синусовом ритме непредсказуемо.
Малоэффективна, по современным представлениям, гидратация с введением больших количеств жидкости (показана лишь регидратация с целью восполнения потерь жидкости с потом или вследствие усиленного диуреза после использования эуфиллина).
Абсолютно недопустимо применение наркотическиих анальгетиков в связи угрозой угнетения дыхательного центра. Не рекомендуется также применение атропина в связи с возможным нарушением дренажной функции бронхов вследствие торможения мукоцилиарной системы и повышения вязкости секрета в бронхах.
Определенными бронхолитическими свойствами обладает сульфат магния, но его применение в качестве средства для купирования приступов БА не рекомендуется.
Приступ удушья нередко сопровождается выраженными эмоциональными расстройствами (страхом смерти и т.п.), но применение транквилизаторов, угнетающих дыхание вследствие центрального миорелаксирующего действия, противопоказано.
Наконец, ошибочной тактикой является применение эуфиллина после адекватной ингаляционной терапии бета-2-агонистами, а также повторные в/в его инъекции (особенно у пациентов, получающих пролонгированные теофиллины) - риск развития побочных эффектов (тахикардия, аритмия) от подобного лечения превышает пользу от введения эуфиллина. Позднее назначение глюкокортикоидов (нередко в неадекватных дозах) в этой ситуации бывает обусловлено преувеличенным страхом перед их использованием.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ:
Госпитализация показана больным при тяжелом обострении БА и угрозе остановки дыхания; при отсутствии быстрого ответа на бронходилатационную терапию или при дальнейшем ухудшении состояния больного на фоне начатого лечения; при длительном использовании или недавно прекращенном приеме системных кортикостероидов. Также в стационар должны направляться пациенты, несколько раз госпитализировавшиеся в отделение интенсивной терапии в течение последнего года; пациенты, не придерживающиеся плана лечения БА и пациенты, страдающие психическими заболеваниями.
Клинический пример эффективности небулайзерной терапии.
5.2 ПНЕВМОНИЯ
ОПРЕДЕЛЕНИЕ.
Пневмония (П) - острое инфекционное заболевание преимущественно бактериальной этиологии, характеризующееся очаговым поражением респираторных отделов легких с внутриальвеолярной экссудацией, выявляемой при физикальном и/или рентгенологическом исследовании и выраженными в различной степени лихорадочной реакцией и интоксикацией.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ.
П вызываются инфекционным агентом. Наиболее часто это пневмококки, палочка инфлюэнцы, стрептококки, стафилококки, микоплазмы и хламидии. Широкое и не всегда оправданное применение антибиотиков, особенно широкого спектра действия, привело к селекции резистентных штаммов и развитию антибиотикорезистентности. Вирусы также способны вызывать воспалительные изменения в легких, воздействуя на трахеобронхиальное дерево, создают условия для проникновения в респираторные отделы легких пневмотропных бактериальных агентов.
Основным путем заражения является воздушно-капельный путь проникновения возбудителей или аспирация содержащего микроорганизмы секрета из верхних отделов дыхательных путей.
Реже встречается гематогенный путь распространения возбудителей ( эндокардит трикуспидального клапана, септический тромбофлебит вен таза) и непосредственное распространение инфекции из соседних тканей ( абсцесс печени) или инфицирование при проникающих ранениях грудной клетки.
КЛИНИЧЕСКАЯ КАРТИНА И КЛАССИФИКАЦИЯ.
В зависимости от условий возникновения, клинического течения, состояния иммунологической реактивности больного выделяют следующие виды П:
- внебольничная ( домашняя, амбулаторная)
- госпитальная ( нозокомиальная, внутрибольничная)
-аспирационная
- на фоне иммунодефицитных состояний
Эта классификация используется для обоснования эмпирической терапии. Детализация П с учетом факторов риска ( хроническая алкогольная интоксикация, на фоне ХОБЛ, вирусных инфекций, злокачественных и системных заболеваний, ХПН, предшествующей антибиотикотерапии и т. п. , позволяет учитывать весь спектр возможных возбудителей и повышает адресность стартовой антибиотикотерапии
Клиническая картина П определяется как особенностями возбудителя, так и состоянием пациента и складывается из внелегочных симптомов и признаков поражения легких и бронхов.
Клинические симптомы пневмонии.
1) Бронхолегочные: кашель, одышка, боли в грудной клетке, отделение мокроты, иногда кровохарканье, притупление перкуторного звука, ослабление везикулярного или бронхиального дыхания, крепитация, шум трения плевры;
2) Внелегочные: гипотензия, слабость, тахикардия, потливость, озноб, лихорадка, спутанность сознания, острый психоз, менингиальные симтомы, декомпенсация хронических заболеваний
У пациентов с хронической алкогольной интоксикацией или тяжелыми сопутствующими заболеваниями ( сахарным диабетом, застойной сердечной недостаточностью, инфарктом мозга и т.п.) или у пожилых внелегочные симптомы могут превалировать над бронхолегочными.
При локализации П в нижних отделах легких и при вовлечении в процесс диафрагмальной плевры ( при крупозной пневмонии - плевропневмонии) боль может иррадиировать в брюшную полость, имитируя картину острого живота.
Плевропневмонию в ряде случаев приходится дифференцировать от инфаркта легкого, для которого так же характерно внезапное появление болевого синдрома, нередко кровохарканье, удушье. Однако в начале болезни непатогномоничны наличие высокой температуры, интоксикация. У этих пациентов удается выявить возможные источники тромбоэмболии (тромбофлебит нижних конечностей, порок сердца, постинфарктный кардиосклероз). При регистрации ЭКГ выявляются симптомы перегрузки правого сердца ( блокада правой ножки пучка Гиса, признак SI-QIII. ).
При спонтанном пневмотораксе острое развитие болевого синдрома может сочетаться с нарастающей дыхательной недостаточностью (напряженный спонтанный пневмоторакс). При перкуссии выявляется тимпанит, ослабление дыхания, иногда увеличение объема и ограничение дыхательных экскурсий соответствующей половины грудной клетки.
Осложнениями П являются плеврит, абсцедирование, пиопневмоторакс и эмпиема плевры, респираторный дистресс-синдром взрослых, инфекционно-токсический шок, бронхообструктивный синдром, сосудистая недостаточность. При тяжелом течении с выраженной интоксикацией, у ослабленных больных возможно развитие сепсиса, инфекционного эндокардита, поражения миокарда и почек.
Крупозная пневмония, облигатно связанная с пневмококковой инфекцией, является одной из самых тяжелых форм П. Для нее характерны: острое начало заболевания с потрясающим ознобом, кашель, боль в грудной клетке при дыхании, ржавая мокрота, отчетливые перкуторные и аускультативные изменения в легких, критическое падение температуры тела; возможно развитие гипотензии, острой сосудистой недостаточности, респираторного дистресс - синдрома взрослых, инфекционно-токсического шока.
При стафилококковых П, которые чаще встречаются в
период эпидемии гриппа, развиваются тяжелая интоксикация, гнойные осложнения.
У пожилых и у лиц с алкогольной зависимостью часто вызываются грамотрицательной
флорой, в частности Klebsiella pneumoniae. При этих П наблюдается обширное
поражение легочной ткани с деструкцией, гнойные осложнения, интоксикация.
ПЕРЕЧЕНЬ ВОПРОСОВ БОЛЬНОМУ С ПНЕВМОНИЕЙ.
1) Время начала заболевания.
2) Наличие факторов риска, отягощающих течение П
Хронические заболевания, вредные привычки и т.д.
3) Выяснение эпидемиологического анамнеза.
Выявление признаков возможного инфекционного заболевания.
4)Длительность и характер повышения температуры.
5) Наличие кашля, мокроты, ее характера, кровохарканья.
6) Наличие боли в грудной клетке, ее связи с дыханием, кашлем
7) Есть ли одышка, приступы удушья
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ ПНЕВМОНИИ.
1. Жалобы больного на кашель, отделение мокроты, боли в грудной клетке, одышку
2. Острое начало заболевания
3. Изменения при перкуссии (притупление перкуторного звука) и аускультации (ослабление везикулярного дыхания, бронхиальное дыхание, крепитация, шум трения плевры ) легких, проявления бронхообструкции
4. Повышение температуры
5. Симптомы интоксикации
При осмотре пациента необходимо измерить температуру, частоту дыхания, АД, ЧСС; провести пальпацию живота, выявить симптомы декомпенсации сопутствующих заболеваний.
При подозрении на ОИМ, ТЭЛА, в пожилом возрасте, при сопутствующем атеросклерозе необходимо провести ЭКГ исследование.
Выявление пневмонической инфильтрации при рентгенографическом исследовании подтверждает диагноз П.
Данные лабораторных исследований (анализ периферической крови, биохимические исследования), определение газового состава крови важны для оценки тяжести состояния больного и выбора терапии.
Цитологическое исследование мокроты позволяет уточнить характер воспалительного процесса и его выраженность.
Бактериологическое исследование мокроты, бронхиального содержимого, крови важно для коррекции антибактериальной терапии, особенно при тяжелых П.
Клинический пример . Больной В., 44 лет, вызвал бригаду СС и НМП в связи с внезапным появлением озноба, повышением температуры до 38,5, резкими болями справа в боку, усиливающимися при дыхании и движении. В анамнезе злоупотребление алкоголем.
Был госпитализирован с диагнозом “острый холецистит”. При осмотре в приемном отделении хирургическая патология была исключена, но было выявлено притупление перкуторного звука справа в нижних отделах легких, там же усиление дыхания и бронхофонии. Врач приемного отделения заподозрил пневмонию. При рентгенологическом исследовании был подтвержден диагноз нижнедолевой провосторонней плевропневмонии. Таким образом, в данном случае у больного с правосторонней плевропневмонией плевральные боли иррадиировали в правое подреберье и имитировали картину острого холецистита.
Для врача СиНМП большое значение имеет деление П по степени тяжести, что позволяет выделить больных, нуждающихся в госпитализиции и в проведении интенсивной терапии на догоспитальном этапе. Основными клиническими критериями тяжести заболевания являются степень дыхательной недостаточности, выраженность интоксикации, наличие осложнений, декомпенсация сопутствующих заболеваний.
Критерии тяжелой пневмонии (Niederman et al., 1993).
1. ЧДД > 30 в минуту.
2. Температура выше 38,5 С
3. Внелегочные очаги инфекции
4. Нарушение сознания
5. Необходимость проведения искусственной вентиляции легких
6. Шоковое состояние (САД менее 90 мм.рт.ст. или ДАД менее 60 мм.рт.ст.)
7. Необходимость применения вазопрессоров на протяжении более 4 ч.
8. Диурез < 20 мл/ч или проявления острой почечной недостаточности.
Пациенты, с факторами риска развития осложнений и летального исхода, также подлежат госпитализации.
Факторы риска, повышающие вероятность развития осложнений и смертности от пневмонии (Niederman et al., 1993).
1. Хронические обструктивные заболевания легких
2. Сахарный диабет
3. Хроническая почечная недостаточность
4. Левожелудочковая сердечная недостаточность
5. Хроническая печеночная недостаточность
6. Госпитализации в течение предшествующего года.
7. Нарушение глотания
8. Нарушение высших нервных функций
9. Спленэктомия
10.Алкоголизм
11.Алиментарное истощение
12.Возраст старше 65 лет
АЛГОРИТМ ТАКТИКИ ВРАЧА СиНМП ПРИ ПНЕВМОНИИ
Больные с П среднего и тяжелого течения, при осложненном течении, при наличии факторов риска, подлежат госпитализации. У ряда пациентов на догоспитальном этапе могут развиться симптомы, требующие коррекции врачом СиНМП.
АЛГОРИТМ ТАКТИКИ ВРАЧА СиНМП ПРИ ПНЕВМОНИИ
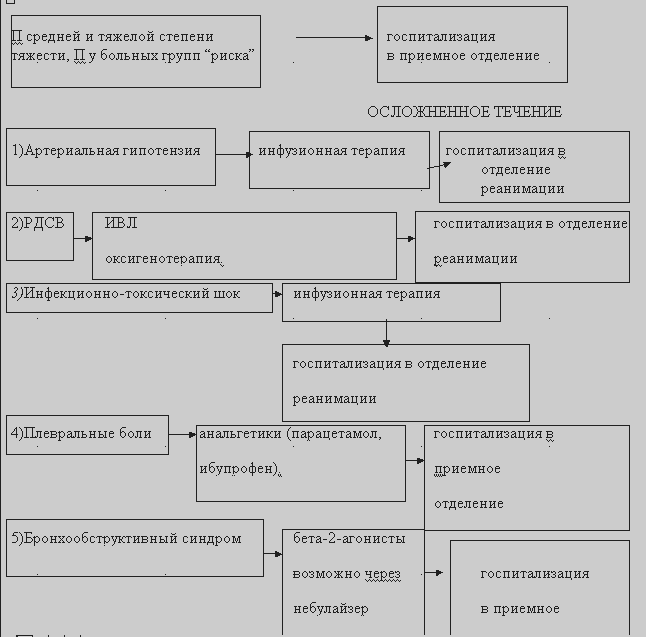
Артериальная гипотензия у больных с крупозной П ( плевропневмонией) возникает вследствие генерализованного снижения тонуса гладкой мускулатуры стенок артериол и мелких артерий и снижения общего периферического сопротивления. По мнению ряда авторов причиной этого является немедленный ответ сосудистой стенки при анафилактической реакции сенсибилизированного организма на продукты распада пневмококка, которые в данном случае действуют не как токсины, а как антигены.. Больных крупозной П необходимо госпитализировать в терапевтические отделения в положении лежа. Не следует начинать до госпитализации антибактериальную терапию, назначать жаропонижающие или анальгетические препараты, так как это может привести к падению АД, что особенно опасно при транспортировке больного.
Для обеспечения поддержания САД на уровне 100 мм.рт.ст. проводится введение жидкостей (в/в капельно изотонические растворы натрия хлорида, декстрозы, декстрана 40 в общем объеме 500 - 1000 мл).
Острая дыхательная недостаточность - респираторный дистресс-синдром взрослых (РДСВ). РДСВ чаще развивается при сепсисе, бактериальном шоке, у больных П на фоне иммунодефицита (хроническая алкогольная интоксикация, нейтропения, наркотическая зависимость, ВИЧ-инфицирование). В ответ на инфекцию развивается местная воспалительная реакция, приводящая к вазодилатации, увеличению проницаемости сосудистой стенки, высвобождению ряда клеточных компонентов (лизосомальных ферментов, вазоактивных аминов, простагландинов), активируется система комплемента, привлекающая нейтрофилы в легочную микроциркуляцию. Гранулоциты и мононуклеары накапливаются в месте повреждения и образуют конгломерат с местными фибробластами и эндотелиальными клетками. Адгезия нейтрофилов к эндотелию стимулирует высвобождение повреждающих его токсических субстанций. В результате поражения эндотелия легочных капилляров развивается отек легких, клинически проявляющийся тяжелой одышкой и выраженной гипоксемией, устойчивой к оксигенотерапии, что обусловливает повышенную потребность в кислороде. Больные нуждаются в ИВЛ. Диуретики малоэффективны при отеке легких у больных с РДСВ. Введение фуросемида в/в может способствовать улучшению газообмена без уменьшения степени отека легких, что, возможно объясняется перераспределением легочного кровотока (увеличением его в хорошо вентилируемых участках легких).
Основной задачей терапии при лечении дыхательной недостаточности является поддержание оксигенации тканей. При РДСВ потребление кислорода на периферии прямо пропорционально его доставке. При артериальной гипотензии и снижении сердечного выброса показана в/в инфузия добутамина в дозе 5 - 10 мкг/кг мин.
Периферические вазодилататоры усугубляют легочную гипоксемию, увеличивая внутрилегочное шунтирование. Насыщение гемоглобина артериальной крови кислородом поддерживают выше 90%, что достаточно для поддержания доставки кислорода периферическим тканям. В настоящее время не доказанным считается то, что применение глюкокортикостероидов в высоких дозах ослабляет воспалительный процесс в легких. В то же время высокие дозы глюкокортикостероидов повышают риск развития вторичной инфекции.
Инфекционно - токсический шок может осложнять течение крупозной (плевропневмонии), стафилококковой П, встречается при П., вызванных грамотрицательной флорой и у больных с факторами риска. Лечение на догоспитальном этапе заключается в инфузионной терапии, введении добутамина. Более подробно - см. соответствующий раздел.
Бронхообструктивный синдром - см. соответствующий раздел.
Плевральные боли иногда выражены столь сильно, что требуют введения анальгетиков. Наиболее рационально использование препаратов из группы НПВС (парацетамол 0,5 г per os, ибупрофен - 0,2 г per os; аспирин 0,5 - 1,0 г. per os или парентерально в форме лизинмоноацетилсалицилата 2,0 г.; диклофенак - 0,075 г per os или парентерально в/м глубоко в ягодичную мышцу 0,075 г). Анальгин, который до настоящего времени широко используется как анальгетик, значительно чаще вызывает серьезные нежелательные эффекты (острую анафилаксию, угнетение гемопоэза ) и поэтому не может быть рекомендован к применению.
У больных с крупозной П (плевропневмонией) введение анальгетиков может спровоцировать гипотензию и от их применения на догоспитальном этапе лучше воздержатся.
ПАРАЦЕТАМОЛ. Максимальная концентрация в крови достигается через 0,5-2 ч. после приема, продолжительность действия составляет 3-4 ч.
Показаниями к применению являются легкая и умеренно выраженная боль, температура выше 38 С.
При заболеваниях печени и почек, хронической алкогольной интоксикации препарат следует применять с осторожностью.
Противопоказаниями являются реакции гиперчувствительности на препарат в анамнезе.
Нежелательные эффекты (развиваются редко): кожная сыпь, цитопении, повреждение печени (реже - почек ) при передозировке, особенно на фоне приема алкоголя. При длительном применении возможно развитие острого панкреатита.
При сочетанном применении с прокинетиками и длительном совместном применении с непрямыми антикоагулянтами возможно усиление действия прокинетиков и антикоагулянтов.
Дозы: взрослым назначают внутрь 0,5-1,0 г каждые 4 - 6 часов, максимальная суточная доза - 4 г.
АСПИРИН ( ацетилсалициловая кислота). Максимальная концентрация в крови достигается через 2 ч. после приема. Продолжительность действия 4 ч.
Показания: легкая и умеренно выраженная боль, температура выше 38 С
При БА, аллергических реакциях в анамнезе, заболеваниях печени и почек, дегидратации, в период беременности и у пожилых пациентов препарат следует применять с осторожностью.
У детей моложе 12 лет, кормящих матерей, при язвенной болезни, гемофилии, гиперчувствительности к аспирину и другим НПВП, выраженной почечной и печеночной недостаточности и в 3-ем триместре беременности применение аспирина противопоказано.
К нежелательным эффектам относятся желудочно-кишечная диспепсия, бронхоспазм, кожные реакции. При длительном приеме возможно ульцерогенное действие, увеличение времени кровотечения, тромбоцитопения, реакции гиперчувствительности.
При сочетании с другими НПВП и глюкокортикостероидами увеличивается риск развития нежелательных эффектов, с антикоагулянтами - увеличение риска кровотечений. Сочетанное применение с цитостатиками и противоэпилептическими средствами увеличивает токсичность этих препаратов.
Дозы: взрослые - 0,25 - 1,0 г каждые 4 - 6 часов, максимальная доза 4 г/день.
Применение у детей не рекомендуется.
Лизинмоноацетилсалицилат - производное аспирина для парентерального введения. Превосходит его по быстроте развития и силе анальгезирующего эффекта. Разовая доза 2 г, максимальная - до 10 г в сутки. Нежелательные реакции - аналогичные действию аспирина.
ИБУПРОФЕН Максимальная концентрация в крови развивается через 1-2 ч после приема внутрь, анальгезирующий и жаропонижающий эффекты длятся до 8 часов. Ибупрофен назначают при легкой и умеренно выраженной боли, температуре выше 38 С
С осторожностью рекомендуется применять у пожилых, при аллергических реакциях в анамнезе, беременности, лактации, нарушениях коагуляции, нарушениях функции печени и почек, БА.
Противопоказаниями являются гиперчувствительность к НПВП, тяжелая почечная и печеночная недостаточность, язвенная болезнь, третий триместр беременности.
Нежелательные эффекты: желудочно-кишечная диспепсия, реакции гипечувствительности, бронхоспазм; цитопении, аутоиммунные синдромы, при курсовом приеме ульцерогенное действие, усугубление почечной и печеночной недостаточности, головная боль, головокружения, нарушение слуха, ориентации, фотосенсибилизация, редко папиллярный некроз, асептический менингит.
Сочетанное применение с другими НПВП и глюкокортикостероидами повышает риск развития нежелательных эффектов. При сочетании с фторхинолонами возможно возможно развитие судорожного синдрома. При сочетанном применении с диуретиками, ингибиторами АПФ, бета-блокаторами наблюдается снижение терапевтического эффекта этих препаратов и увеличение риска развития побочных эффектов. При сочетании с цитостатиками, противоэпилептическими средствами, препаратами лития повышаются их эффекты; при сочетании с антикоагулянтами увеличивается риск геморрагических осложнений, при сочетании с сердечными гликозидами НПВП могут увеличивать их плазменную концентрацию.
Рекомендуется прием 1,2-1,8 г в день в 3 - 4 приема, максимальная суточная доза - 2,4 г.
ДИКЛОФЕНАК. Максимальная концентрация в крови развивается через 0,5 - 2 час. после приема внутрь и через 10 - 30 мин. после в/м введения.
Показания - см. выше
Противопоказания: см. выше, а также обострение хронических заболеваний кишечника, порфирия.
Взаимодействия: типичны для препаратов группы НПВС (см. выше).
Дозы: 75 - 150 мг/сут в два - три приема внутрь, в/м 75 мг глубоко в ягодичную мышцу.
Своевременно начатая антибиотикотерапия оказывает решающее влияние на течение П и ее исход. При поступлении больного в стационар выбор антибиотика осуществляют с учетом вышеприведенных клинических особенностей.
АНТИБИОТИКОТЕРАПИЯ ПРИ ПНЕВМОНИЯХ.
|
Клиническая ситуация |
Наиболее частые возбудители |
Антибиотики первого ряда |
|
П нетяжелого течения у пациентов моложе 60 лет с неотягощенным анамнезом |
S. pneumoniae, M. pneumoniae, H. influenzae
|
Аминопенициллины, макролиды |
|
П у пациентов 60 лет и старше и/или с сопутствующей патологией |
S. pneumoniae, H. influenzae, Enterobacteriaceae
|
Амоксициллин - - клавуланат ( + аминогликозиды), цефалоспорины II поколения ( + аминогликозиды)
|
|
П тяжелого течения |
S. pneumoniae, Enterobacteriaceae, Staphylococcus aureus, Legionella spp. |
Цефалоспорины III поколения ( +аминогликозиды, оксациллин), + макролиды фторхинолоны |
|
П у пациентов с иммунодифицитом |
Enterobacteriaceae, Pseudomonas spp., S. pneumoniae, Staphylococcus aureus, грибы |
Фторхинолоны (+аминогликозиды, ванкомицин), антисинегнойные цефалоспорины III поколения (антисинегнойные пенициллины) + аминогликозиды, ванкомицин, амфотерицин, дифлюкан |
|
Аспирационные П |
S. pneumoniae, Staphylococcus, Enterobacteriaceae, анаэробы |
Цефалоспорины III поколения (+аминогликозид), амоксициллин - клавуланат + аминогликозид, фторхинолоны, метронидазол |
5.3 ТРОМБОЭМБОЛИЯ ЛЕГОЧНОЙ АРТЕРИИ
ОПРЕДЕЛЕНИЕ.
Тромбоэмболия легочной артерии (ТЭЛА) представляет собой синдром, обусловленный эмболией легочной артерии или ее ветвей тромбом и характеризуется резкими кардиореспираторными расстройствами, а при перекрытии небольших ветвей - симптомами образования геморрагических инфарктов легкого.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ.
Наиболее частой причиной и источником эмболизации ветвей легочной артерии являются тромбы из глубоких вен нижних конечностей при флеботромбозе (около 90% случаев), значительно реже - из правых отделов сердца при сердечной недостаточности и перерастяжении правого желудочка. Предрасполагающими факторами являются длительная неподвижность, операции на тазовых органах или нижних отделах брюшной полости, травма, ожирение, прием оральных контрацептивов, беременность, злокачественные новообразования, инфаркт миокарда, дилатационная кардиомиопатия, застойная сердечная недостаточность, мерцательная аритмия, сепсис, инсульт, травма спинного мозга, эритремия, нефротический синдром.
КЛИНИЧЕСКАЯ КАРТИНА, КЛАССИФИКАЦИЯ И ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ.
Патогномоничных для ТЭЛА клинических признаков не существует, диагноз на догоспитальном этапе может быть заподозрен на основании совокупности анамнестических данных, результатов объективного обследования и электрокардиографических симптомов.
КЛИНИКО-ЭЛЕКТРОКАРДИОГРАФИЧЕСКАЯ КАРТИНА ТЭЛА.
|
Клинические признаки |
Внезапное начало с появлением одышки (72% случаев) и острой боли в груди (86%), часто - острая сосудистая недостаточность с появлением бледности, цианоза, тахикардии (87%), падением АД вплоть до развития коллапса и потери сознания (12%). При развитии инфаркта легкого в 10-50% случаев появляется кровохарканье в виде прожилок крови в мокроте. При осмотре могут определяться признаки легочной гипертензии и острого легочного сердца - набухание и пульсация шейных вен, расширение границ сердца вправо, пульсация в эпигастрии, усиливающаяся на вдохе, акцент и раздвоение II тона на легочной артерии, увеличение печени. Возможно появление сухих хрипов над легкими. |
|
ЭКГ-признаки (появляются в 25% случаев). |
Признаки перегрузки правого предсердия (P-pulmonale - высокий заостренный зубец P в отведениях II, III, aVF) и правого желудочка (синдром Мак-Джина-Уайта - глубокий зубец S в I отведении, глубокий зубец Q и отрицательный зубец Т в III отведении с возможным подъемом сегмента SТ; неполная блокада правой ножки пучка Гиса), |
Таким образом, несмотря на отсутствие четких диагностических критериев, ТЭЛА может быть диагностирована на догоспитальном этапе на основе тщательной комплексной оценки анамнеза, данных осмотра и ЭКГ. Окончательная верификация диагноза проводится в стационаре. Иногда при рентгенологическом исследовании выявляются высокое стояние купола диафрагмы, дисковидный ателектаз, полнокровие одного из корней легких или "обрубленный" корень, обеднение легочного рисунка над ишемизированной зоной легкого, периферическая треугольная тень воспаления или плевральный выпот, но у большинства пациентов какие-либо рентгенологические изменения отсутствуют. Диагноз подтверждается перфузионной сцинтиграфией легких, позволяющей обнаружить характерные треугольные участки снижения перфузии легких (метод выбора), а также рентгенконтрастной ангиографией легких (ангиопульмонографией), выявляющей зоны редуцированного кровотока.
Клинически различают острое, подострое и рецидивирующее течение ТЭЛА (табл. 13.).
ВАРИАНТЫ ТЕЧЕНИЯ ТЭЛА.
|
Течение ТЭЛА |
Характерные клинические особенности |
|
Острое |
Внезапное начало, боль за грудиной, одышка, падение АД, признаки острого легочного сердца |
|
Подострое |
Прогрессирующая дыхательная и правожелудочковая недостаточность, признаки инфарктной пневмонии, кровохарканье |
|
Рецидивирующее |
Повторные эпизоды одышки, обмороки, признаки пневмонии |
При анализе клинической картины врач СиНМП должен получить ответы на следующие вопросы.
1) Имеется ли одышка, если да - то как она возникла (остро или постепенно).
При ТЭЛА одышка возникает остро, ортопноэ не характерно.
2) Есть ли боль в грудной клетке.
Может напоминать стенокардию, локализуясь за грудиной, может усиливаться при дыхании и кашле.
3) Не было ли немотивированных обмороков.
ТЭЛА сопровождается или проявляется синкопе примерно в 13 % случаев.
4) Есть ли кровохарканье.
Появляется при развитии инфаркта легкого.
5) Бывают ли отеки ног (обращая внимание на их асимметричность).
Тромбоз глубоких вен голеней - частый источник ТЭЛА.
6) Не было ли недавних операций, травм, нет ли заболеваний сердца с застойной сердечной недостаточностью, нарушениями ритма, не принимает ли пероральные контрацептивы, нет ли беременности, не наблюдается ли у онколога.
Наличие предрасполагающих факторов ТЭЛА (например, пароксизмальной мерцательной аритмии) должно учитываться врачом при возникновении у пациента острых кардио-респираторных расстройств.
АЛГОРИТМ ЛЕЧЕНИЯ ТЭЛА
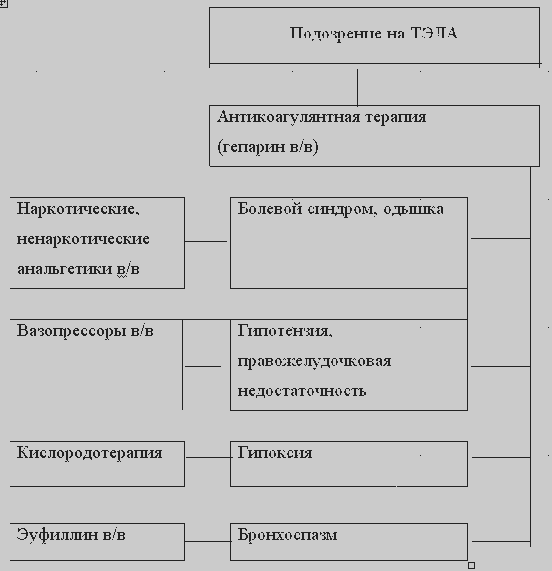
Основные направления терапии ТЭЛА на догоспитальном этапе включают купирование болевого синдрома, профилактику продолженного тромбоза в легочных артериях и повторных эпизодов ТЭЛА, улучшение микроциркуляции (антикоагулянтная терапия), коррекцию правожелудочковой недостаточности, артериальной гипотензии, гипоксии (кислородотерапия), купирование бронхоспазма.
При выраженном болевом синдроме и для разгрузки малого круга кровообращения и уменьшения одышки используют наркотические анальгетики (например, 1 мл 1% раствора морфина в/в дробно). Это позволяет не только эффективно купировать болевой синдром, но и уменьшить характерную для ТЭЛА одышку. Побочные эффекты и противопоказания к применению морфина см. в разделе “Инфаркт миокарда”.
При развитии инфарктной пневмонии, когда боль в грудной клетке связана с дыханием, кашлем, положением тела, более целесообразно использование ненаркотических анальгетиков (например, внутривенное введение 2 мл 50% раствора анальгина).
Выживаемость пациентов при инфаркте легкого напрямую зависит от возможности раннего применения антикоагулянтов. Целесообразно применение прямых антикоагулянтов - гепарина в/в струйно в дозе 10000-20000 МЕ. Гепарин не лизирет тромб, но приостанавливает тромботический процесс и препятствует нарастанию тромба дистальнее и проксимальнее эмбола. Ослабляя сосудосуживающее и бронхоспатическое действие торомбоцитарного серотонина и гистамина, гепарин уменьшает спазм легочных артериол и бронхиол, благоприятно влияя на течение флеботромбоза, гепарин служит для профилактитки рецидивов ТЭЛА. Побочные эффекты и противопоказания к применению гепарина см. в разделе “Инфаркт миокарда”.
При осложнении течения заболевания правожелудочковой недостаточностью, гипотензией или шоком показана терапия допамином или добутамином (см. раздел "Шок"). Для улучшения микроциркуляции дополнительно используют реополиглюкин - 400 мл вводят внутривенно капельно со скоростью до 1 мл в мин. Реополиглюкин не только увеличивает ОЦК и повышает артериальное давление, но и обладает антиагрегационным действием. При сохраняющемся на фоне указанного лечения шоке переходят к терапии прессорными аминами - 200 мг допамина разводят в 400 мл реополиглюкина, при этом в 1 мл полученного раствора содержится 500 мкг допамина, в одной капле - 25 мкг. Начальная скорость введения 5 мкг/кг мин под контролем АД с постепенным повышением дозы до 15 мкг/кг мин. 2 мл 0,2% раствора норадреналина разводят в 250 мл изотонического раствора натрия хлорида и вводят с начальной скоростью 40-50 капель в минуту (при стабилизации гемодинамики скорость уменьшают до 10-20 капель в минуту).
При ТЭЛА показана длительная кислородотерапия. При развитии бронхоспазма и стабильном АД (САД не ниже 100 мм рт. ст.) показано в/в медленное (струйное либо капельное) введение 10 мл 2,4% раствора эуфиллина. Эуфиллин снижает давление в легочной артерии, обладает антиагрегантными свойствами, оказывает бронходилатирующее действие.
ЧАСТО ВСТРЕЧАЮЩИЕСЯ ОШИБКИ ТЕРАПИИ.
При инфаркте легкого у больных с ТЭЛА нецелесообразно применение кровоостанавливающих средств, поскольку кровохарканье появляется на фоне тромбоза или тромбоэмболии.
Нецелесообразно также назначение сердечных гликозидов при острой правожелудочковой недостаточности, поскольку эти препараты не влияют изолированно на правые отделы сердца и не уменьшают постнагрузку на правый желудочек. Дигитализация, однако, вполне оправдана у пациентов с тахисистолической формой мерцательной аритмии, нередко являющейся причиной тромбоэмболии.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ.
При подозрении на ТЭЛА госпитализация обязательна.
5.4 ГНОЙНЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ.
Острый абсцесс, гангрена легкого
ОПРЕДЕЛЕНИЕ
Острый абсцесс, гангрена легкого представляют собой гнойно-некротическое расплавление легочной паренхимы (при гангрене некроз более обширный, без четких границ, имеющий тенденцию к распространению; клинически заболевание проявляется очень тяжелым общим состоянием пациента).
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ.
Основными причинами возникновения деструктивных изменений в легких являются: осложнение острой П (часто постгриппозной) - в 63-95%случаев; аспирация (попадание инфекционного начала в легкое из полости рта - кариозные зубы, пародонтоз, хронический тонзиллит). В последние годы установлено, что в 50-60% наблюдений аспирируется исключительно анаэробная микрофлора (Fusobact. nucleatum, Fusobact. necrophorum, Bacter. fragilis, Bacter. melaninogenus и др.).
Кроме того, наиболее частыми возбудителями являются: гемолитический стафилококк и грамотрицательная микрофлора.
Среди других причин развития острого абсцесса и гангрены легкого необходимо указать на гематогенно-эмболический путь (в 0,8-9,0 % случаев), посттравматический фактор, обтурацию бронхов (опухолью, инородным телом).
Следует подчеркнуть, что острые абсцессы и гангрена легкого чаще всего развиваются у ослабленных хроническими заболеваниями больных, у лиц с алкогольной зависимостью; при тяжелых системных заболеваниях, на фоне ХНЗЛ.
КЛИНИЧЕСКАЯ КАРТИНА
острых абсцессов и гангрены легкого разнообразна и зависит от размеров некротизированных участков легочной ткани, осложненного или неосложненного течения, возраста пациента, сопутствующей патологии, индивидуальных особенностей организма и т.д. При абсцессе легкого в начальный (первый) период заболевания (до вскрытия абсцесса в бронх) тяжесть состояния больных определяется гнойной интоксикацией из-за невозможной эвакуации гноя и некротических масс из полостей деструкции естественным путем через дренирующие бронхи. Больные жалуются на высокую температуру, ознобы, боли в соответствующей половине грудной клетки, кашель со скудной мокротой. При физикальном исследовании - на "больной" стороне дыхание ослаблено, перкуторный звук укорочен. При большом поражении легочной ткани могут выслушиваться крепитирующие хрипы. Данные рентгенологического исследования свидетельствуют о воспалительной инфильтрации легкого без четких границ.
Первый период болезни продолжается в среднем 7-10 дней.
Во втором периоде заболевания (после вскрытия абсцесса в бронх) патогномоничным симптомом будет обильное отхождение гнойной мокроты, нередко с неприятным запахом, "полным ртом". Если при этом происходит аррозия бронхиальных сосудов, будет отмечаться легочное кровотечение. Одновременно снижается температура, уменьшается интоксикация, улучшается самочувствие. При физикальном исследовании возможно выявление полости в легком при перкуссии, при аускультации - бронхиальное дыхание с амфорическим оттенком. Характерна рентгеносемиотика - округлая полость, окруженная инфильтративным валом, с горизонтальным уровнем жидкости в просвете ее.
Мокрота (макроскопически) имеет три слоя: гной, мутная жидкость, пенистый слой.
Гангрена легкого характеризуется более обширным некрозом легочной паренхимы (чем при абсцессе), без четких границ, занимающим несколько сегментов, долю или целиком легкое. Заболевание протекает бурно, с гектической лихорадкой, выраженной интоксикацией, болями в груди на стороне поражения, одышкой. Выделяется мокрота грязно-серого или бурого (чаще) цвета со зловонным запахом, определяемым на расстоянии, нередко с секвестрами легочной ткани. Иногда заболевание осложняется легочным кровотечением (кровохарканьем), которое может закончиться летальным исходом. Над участком поражения определяется укорочение перкуторного звука и резко ослабленное (или бронхиальное) дыхание. В анализах крови и мокроты изменения, характерные для острого абсцесса, но более выраженные. На рентгенограммах легких выявляется массивная инфильтрация без четких границ, занимающая долю или все легкое. Если появилась полость распада и она сообщается с просветом бронха, то рентгенологически это определяется в виде просветления неправильной формы (одиночного или множественного), возможно с наличием свободных или пристеночных секвестров.
Следует подчеркнуть, что острый абсцесс и гангрена легкого чреваты развитием ряда тяжелых, порой смертельных осложнений: аррозивное кровотечение (особенно при локализации процесса в прикорневых зонах) пиопневмоторакс (при субплевральных абсцессах), сепсис, перикардит, поражение противоположного легкого.
Острый гнойный плеврит
ОПРЕДЕЛЕНИЕ.
Острый гнойный плеврит - воспаление плевры, характеризующееся образованием гнойного экссудата.
Острый гнойный плеврит (эмпиема плевры) может быть первичным (после проникающего ранения груди, операций на легких, диагностической торакоскопии, при наложении искусственного пневмоторакса) или вторичным (при осложнениях гнойно-воспалительных заболеваний легких и вскрытиях субплеврально расположенных абсцессов). В последнем случае наряду с гноем в плевральную полость поступает и воздух (пиопневмоторакс). Бактериальный спектр содержимого плевральной полости у 62,5% больных свидетельствует об ассоциации возбудителей из 2-5 различных видов (стафилококк, протей, кишечная и синегнойная палочка). Бактериологические исследования в 28% случаев выявили различные виды неклостридиальных анаэробов (бактероиды, фузобактерии, путридный стрептококк и др.).
Клиническая картина
острой вторичной эмпиемы плевры характеризуется тем, что воспалительный процесс с легкого (пневмония, абсцесс, каверна, нагноившаяся киста) переходит на плевру, как правило этой же стороны. Отмечаются резкие боли в соответствующей половине грудной клетки, подъем температуры до 38,5-39 С, признаки дыхательной недостаточности (за счет сдавления легкого гноем и гнойно-деструктивных изменений в самой легочной ткани), кашель с выделением гнойной мокроты. При объективном обследовании выявляются симптомы интоксикации, ограничение дыхательных движений одной половины грудной клетки, притупление перкуторного звука и резкое ослабление дыхания (или оно вовсе не проводится, что бывает чаще). Рентгенологическое исследование свидетельствует о затемнении на стороне эмпиемы, смещении средостения в противоположную сторону. При пиопневмотораксе определяют горизонтальный уровень и газ над ним. В зависимости от количества гнойной жидкости в плевральной полости, а соответственно степени коллабирования легкого различают ограниченный, субтотальный и тотальный пиопневмоторакс.
Спонтанный неспецифический пневмоторакс
ОПРЕДЕЛЕНИЕ.
Спонтанный пневмоторакс (СП) представляет собой скопление воздуха в плевральной полости Развивается, как правило, без предшествующих симптомов (среди полного здоровья). Попадание воздуха происходит из дефекта (дефектов) субплеврально расположенных воздушных булл. Большинство исследователей считают, что формирование булл связано с врожденной неполноценностью паренхимы легкого. В последнее время появились сообщения о случаях семейной формы заболевания - наследственный спонтанный пневмоторакс (наследственная эмфизема). Предполагается, что причиной его является дефицит альфа-1-антитрипсина, который наследуется по аутосомно-рецессивному типу. Чаще поражается правое легкое, двусторонний (как правило, попеременный) пневмоторакс наблюдается в 17,7% случаев.
КЛИНИЧЕСКАЯ КАРТИНА
спонтанного пневмоторакса довольно типична: появление резких болей в соответствующей половине грудной клетки (часто без видимой причины), одышка (ее выраженность зависит от степени коллабирования легкого). Боли иррадиируют в плечо, шею, эпигастральную область, за грудину (особенно при левостороннем пневмотораксе), нередко имитируя стенокардию или инфаркт миокарда. При физикальном обследовании выявляется одышка, тимпанит при перкуссии на стороне поражения, ослабление (или отсутствие) дыхания при аускультации. Диагноз уточняется данными рентгенологического исследования: на пораженной стороне наблюдается пневмоторакс различной степени выраженности и легкое коллабировано. При большом пневмотораксе может быть смещение средостения в противоположную сторону. Необходимо тщательное исследование легких для выяснения возможной причины пневмоторакса - буллезная эмфизема, туберкулезная каверна, абсцесс (при этих заболеваниях пневмоторакс является их осложнением). Иногда большие субплеврально расположенные буллы первого сегмента удается определить на рентгенограммах.
ПРИНЦИПЫ ЛЕЧЕБНЫХ МЕРОПРИЯТИЙ.
Вмешательство на догоспитальном этапе сводится к проведению симптоматической терапии.
1) Болевой синдром - перед транспортировкой пациента в стационар при выраженных плевральных болях могут быть введены ненаркотические аналгетики - кетаролак, трамадол. При пневмотораксе интенсивность болевого синдрома может потребовать введения наркотических аналгетиков. Средством выбора в этом случае следует считать 2% раствор промедола. Необходимо учитывать, что более мощные наркотики, морфин и фентанил, оказывают угнетающее влияние на дыхательный центр и могут способствовать усугублению гипоксии.
2) Артериальная гипотензия - транспортировка пациентов в стационар во избежание развития ортостатического коллапса должна осуществляться в положении лежа. При низком АД (САД < 100) целесообразно во время транспортировки проводить в/в инфузию раствора полиглюкина.
3) Дыхательная недостаточность - развивается при массивном поражении легочной ткани. Для уменьшения степени гипоксии во время транспортировки проводится ингаляция увлажненного кислорода через носовые канюли или маску.
4) Нарастание дыхательной недостаточности при пневмотораксе может быть связано с клапанным механизмом его развития. В этом случае напряженный пневмоторакс требует проведения экстренной декомпрессии, которая проводится путем введения одной или нескольких инъекционных игл крупного диаметра в плевральную полость. Проведение этой манипуляции требует предварительного обезболивания введением 1 мл 2% раствора промедола.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ.
Нагноительные заболевания легких как и случаи развития пневмоторакса требуют экстренную госпитализацию пациентов в отделение торакальной хирургии.
